Covid-19 LFA Uncut Foglio
Validazione clinica Risultato
Convalidato Prodotto: COVID-19 test dell'antigene (LFA) da SHENZHEN SEKBIO Co., LTD.
Punto di riferimento del prodotto: COVID-19 RT-PCR
Esperimento 1: (Orofaringea tampone di eluted con abbinato campione estrazione soluzione)
Numero di campioni | RT-PCR Risultati | SEKBIO COVID-19 antigene risultato del test | ||
| CT valori | Risultato | Risultato | La coerenza | |
| 57 | ≤ 30 | 57 positivi | 57 positivi | 100% |
| 82 | ≤ 33 | 82 positivi | 82 positivi | 100% |
| 91 | ≤ 34 | 91 positivi | 90 positivi | 98.90% |
| 149 | ≤ 36 | 149 positivi | 136 positivi | 91.28% |
| 45 | ≥ 40 | 45 negativi | 44 negativi | 97.78% |
Esperimento 2 : (Nasofaringeo tampone/Orofaringea tampone tenuto in UTM)
| Numero di campioni | RT-PCR Risultati | SEKBIO COVID-19 antigene risultato del test | ||
| CT valori | Risultato | Risultato | La coerenza | |
| 52 | ≤ 25.1 | 52 positivi | 52 positivi | 100% |
| 82 | ≤ 34.8 | 82 positivi | 77 positivi | 93.9% |
| 45 | > 40 | 45 negativi | 45 negativi | 100% |
SARS-CoV-2 Antigene Test Rapido Striscia Risultato
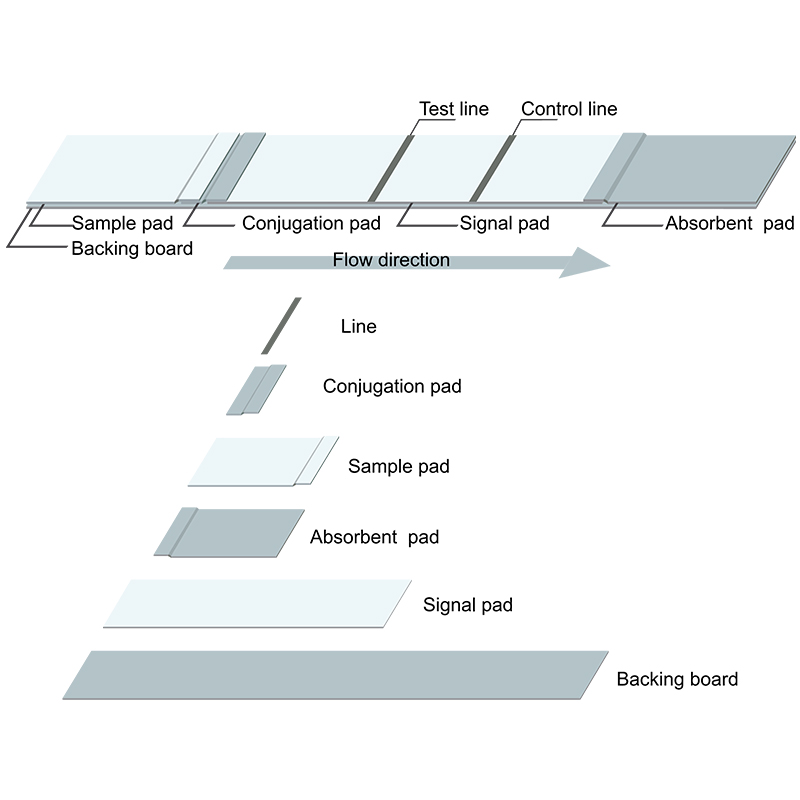
Rapporto di prova del Nuovo Varianti
1. Esperimento scopo:Il COVID-19 ha prodotto una serie di mutazioni durante la pandemia. COVID-19 di rilevamento reagente (flusso laterale cromatografia) è ora utilizzato per rilevare nucleocapsid proteine (NP) le proteine ricombinanti di varianti dal REGNO UNITO, Sud Africa, stati Uniti e Brasile, per verificare le prestazioni della LFA test sul varianti.
2. Materiali esperimento
2.1. COVID-19 NP test reagente (LFA), Lotto N. 2101K402, i risultati del test di NP ricombinante proteina è stato positivo a 31.25pg/ mL e il suo risultato è stato debole positivo a 20pg/mL.
2.2. NP ricombinante proteina del REGNO UNITO variante B.1.1.7, tra cui mutazione: D3L, S235F, espresso in HEK293 cellulare.
2.3. NP ricombinante proteina di South African variante B.1.351, tra cui mutazione: R203K, G204R, espresso in HEK293 cellulare.
2.4. NP ricombinante proteina di NOI variante B.1.2, tra cui mutazione: P67S, P199L, espresso in HEK293 cellulare.
2.5. NP ricombinante proteina di U Brasile variante B.1.1.28, tra cui mutazione: P80R, S235F, espresso in HEK293 cellulare.
3. Metodo di esperimento
3.1. Il NP proteine ricombinanti dei quattro varianti erano diluito con il campione diluente. Il rapporto di diluizione è come segue: 1/1K, 1/200K, 1/400K, 1/800K, 1/1600K, 1/3200K, 1/6400K, 1/12800K, 1/25800K
3.2. Uso COVID-19 test reagente (LFA) per rilevare il di cui sopra diluito campioni. Ogni campione è provato due volte.
3.3. Aggiungere i campioni e interpretare i risultati in base al funzionamento metodi nelle istruzioni.
3.4. Registrare i risultati.
4. Esperimento di risultato
La sperimentale registrare i risultati sono mostrati come segue
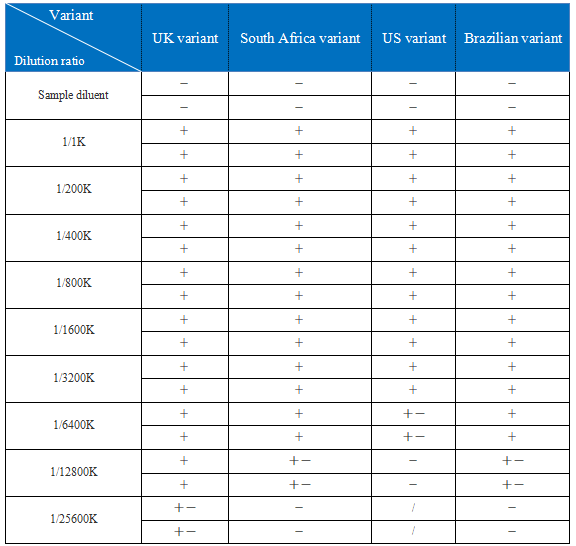
Da la tabella di cui sopra, il risultato del test di NP recomb. Proteine del REGNO UNITO variante è stato positivo a diluizione di 1/12800K e, mentre è stato leggermente positivo A diluizione di 1/25600K. Il risultato del test di NP ricombinante proteina del South African variante è stato positivo a 1/6400K di diluizione E un po 'positivo a 1/12800K di diluizione, mentre è stato negativo a 1/25600K. Il risultato del test di NP ricombinante proteina della American variante è stato positivo a 1/3200K di diluizione e leggermente positivo a 1/6400K di diluizione, mentre è stato negativo a 1/12800K. Il risultato del test di NP ricombinante proteina del Brasiliano variante è stato positivo a diluizione di 1/6400K E un po 'positivo a diluizione di 1/12800K, mentre è stato negativo a 1/25600K.
5. Conclusione esperimento
Il NP ricombinante proteina di la variante dal Regno Unito, Sud Africa, gli stati Uniti e in Brasile è stato rilevabile dal COVID-19 assay (LFA).
Il NP ricombinante proteina del REGNO UNITO variante è rilevabile a il rapporto di diluizione di 1/12800K.
Il NP ricombinante proteina di NOI variante è rilevabile a il rapporto di diluizione di 1/3200K.
Il NP ricombinante proteina di Brasiliani variante è rilevabile a il rapporto di diluizione di 1/6400K.
Il NP ricombinante proteina del Sud Africa variante è rilevabile a il rapporto di diluizione di 1/6400K.

Analisi del potenziale Microbico cross-reazione
Uncut foglio di COVID-19 antigene di rilevamento
Nome del prodotto | Uncut foglio di COVID-19 antigene di rilevamento Romanzo coronavirus (SARS-CoV-2) antigen kit di rilevamento (colloidale oro immunochromatography)-membrana di rilevamento | |||
Spec. | 60 millimetri * 300 millimetri | Lotto N. | 2011K401 | |
Produzione Quantità | 612 pezzi | Di campionamento Quantità | 8 pezzi | |
Produzione Data | 2020-11-01 | Exp. | 2023-04 | |
Deposito a | Sigillato in 2 ⁓ 30 ℃ | Segnalato | 2020-11-02 | |
Di controllo di registrazione | ||||
Elementi di prova | Criteri di accettazione | Risultato | Conclusione | |
Aspetto | Pulito, senza graffi, superficie liscia, nessun danno, senza sbavature, nessun macchie; Ogni supporto del grande bordo deve essere Saldamente incollato. | ☑Soddisfare i requisiti □ Non-compliant | ☑Qualificato □ Non qualificato | |
Lunghezza (Mm) | 300 millimetri ± 3 millimetri | 300 millimetri | ☑Qualificato □ Non qualificato | |
Linea C, T la posizione della linea di | Linea di T, posizione B dovrebbe essere 30mm ± 0.5 millimetri; Linea C B posizione dovrebbe essere 34.5 millimetri ± 0.5 millimetri | Linea di T, posizione B è: 30.0 millimetri linea C, B posizione è: 34.5 millimetri | ☑Qualificato □ Non qualificato | |
Liquido velocità di movimento (Mm/min) | ≥ 10 millimetri/min | 57.5 millimetri/min | ☑Qualificato □ Non qualificato | |
Dissolvenza tempo di pellicola (Min) | 15 ~ 20min | 16 minimo | ☑Qualificato □ Non qualificato | |
Tasso di positivo positivo Di riferimento | Utilizzare il prodotto di riferimento positivo aziendale P1-P5 per testare, Il risultato deve soddisfare il requisito come segue: Il l'intensità del colore di P1 dovrebbe essere C8-C7; | ☑Soddisfare i requisiti □ Non-compliant | ☑Qualificato □ Non qualificato | |
Il l'intensità del colore di P2 dovrebbe essere C6 ~ C5; Il l'intensità del colore di P3 dovrebbe essere C5 ~ C4; Il l'intensità del colore di P4 dovrebbe essere C8 ~ C7; Il l'intensità del colore di P5 dovrebbe essere C7 ~ C6. | ||||
Minimo limite di rilevamento | Uso aziendale più basso limite di rilevamento prodotto di riferimento L1 ⁓ L3 per il test, il risultato deve soddisfare il requisito come segue: Il l'intensità del colore di L1 dovrebbe essere B; Il l'intensità del colore di L2 dovrebbe essere C9 ~ C7; il l'intensità del colore di L3 dovrebbe essere C8 ~ C7. | ☑Soddisfare i requisiti □ Non-compliant | ☑Qualificato □ Non qualificato | |
Di precisione | Uso aziendale ripetibile prodotto di riferimento R1 ⁓ R2 per testare, E il risultato deve soddisfare il requisito come segue: il l'intensità del colore di R1 dovrebbe essere C6 ~ C5; Il l'intensità del colore di R2 dovrebbe essere C7 ~ C6. | ☑Soddisfare i requisiti □ Non-compliant | ☑Qualificato □ Non qualificato | |
Tasso negativo di Negativo Di riferimento | Prova aziendale negativo prodotto di riferimento N1 ⁓ N7, tutti i colori di intensità dovrebbe essere B. | ☑Soddisfare i requisiti □ Non-compliant | ☑Qualificato □ Non qualificato | |
Casuale Clinica Del Campione | Campionamento 100 campioni a caso, con il campione di estrazione soluzione per elute il campione e di test, la prova l'intensità del colore dovrebbe essere B ~ C9. Campionamento 20 campioni a caso in UTM tubo con COPAN conserve di soluzione, e di test, la prova l'intensità del colore dovrebbe essere B ~ C9. | Il numero di l'intensità del colore di B ~ C9/totale numero di prove: 1 20 / 120 | ☑Qualificato □ Non qualificato | |
Il totale tasso di falsi positivi deve essere ≤ 2% | Totale tasso di falsi positivi: 0 | ☑Qualificato □ Non qualificato | ||
Nota | / | |||
Conclusione: | ☑□ Qualificato Non Qualificato | |||















